京药监发〔2024〕96号
各有关单位:
为进一步加强京津冀药物临床试验机构监督管理,提升药物临床试验质量管理水平,依据相关法律、法规和规范性文件,三地药品监管部门联合制定《京津冀药物临床试验机构监督检查标准(2024年版)》,自本通知发布之日起施行。《北京市药品监督管理局天津市药品监督管理局河北省药品监督管理局关于做好药物临床试验机构高质量监管工作的通知》(京药监发〔2021〕170号)同时废止。
特此通知。
北京市药品监督管理局
天津市药品监督管理局
河北省药品监督管理局
2024年4月18日
京津冀药物临床试验机构监督检查标准(2024年版)
为加强京津冀药物临床试验机构监督管理,提升药物临床试验质量管理水平,根据《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》《药品注册管理办法》《药物临床试验质量管理规范》(GCP)《药物临床试验机构管理规定》(以下简称《规定》)《药物临床试验机构监督检查办法(试行)》(以下简称《办法》)《药物临床试验机构监督检查要点及判定原则(试行)》《药品注册核查要点与判定原则(药物临床试验)(试行)》等,结合实际,制订本检查标准。
一、适用范围
本检查标准适用于京津冀药品监督管理部门组织的对行政区域内药物临床试验机构进行的日常监督检查(包括备案后首次监督检查)、有因检查、其他检查。根据检查类型和检查重点,现场检查可适用于部分检查项目。
二、检查内容
检查标准共19个检查环节、147个检查项目,分为机构和临床试验专业(以下简称专业)2个部分,包含对资质条件与备案、运行管理等方面的现场检查内容。检查项目中关键项目共计14项(标示为“★★”),主要项目共计59项(标示为“★”),一般项目共计74项。
三、判定原则
检查发现的缺陷分为严重缺陷、主要缺陷和一般缺陷。一般情况下,关键项目不符合要求判为严重缺陷,主要项目不符合要求判为主要缺陷,一般项目不符合要求判为一般缺陷;可以综合相应检查项目的重要性、偏离程度以及质量安全风险进行缺陷分级。应当对机构和专业分别作出结论。
(一)现场检查结论的判定原则
1.未发现严重缺陷和主要缺陷,发现的一般缺陷少于5项,经综合研判,所发现缺陷不影响受试者安全和/或试验数据质量或者影响轻微,认为质量管理体系比较健全的,结论为符合要求。
2.未发现严重缺陷和主要缺陷,发现的一般缺陷多于或等于5项;或者未发现严重缺陷,但存在主要缺陷且数量少于或等于3项,经综合研判,所发现缺陷可能影响受试者安全和/或试验数据质量,但认为质量管理体系基本健全的,结论为待整改后评定。
3.属于以下情形之一,经综合研判,所发现缺陷可能严重影响受试者安全和/或试验数据质量,认为质量管理体系不能有效运行或者不符合机构备案基本条件的,结论为不符合要求:
(1)严重缺陷1项及以上;
(2)未发现严重缺陷,但主要缺陷3项以上;
(3)其他不符合要求的情形。
(二)综合评定结论的判定原则
1.发现缺陷不影响受试者安全和/或试验数据质量或者影响轻微,认为质量管理体系比较健全的,结论为符合要求。
2.发现缺陷可能严重影响受试者安全和/或试验数据质量,认为质量管理体系不能有效运行或者不符合机构备案基本条件的,结论为不符合要求。
发现缺陷可能影响受试者安全和/或试验数据质量,现场检查结论为“待整改后评定”,整改后仍不能达到符合要求标准的,结论为不符合要求。
四、检查标准内容
详见附表1和附表2。
附表1
京津冀药物临床试验机构监督检查标准——机构部分(A表)
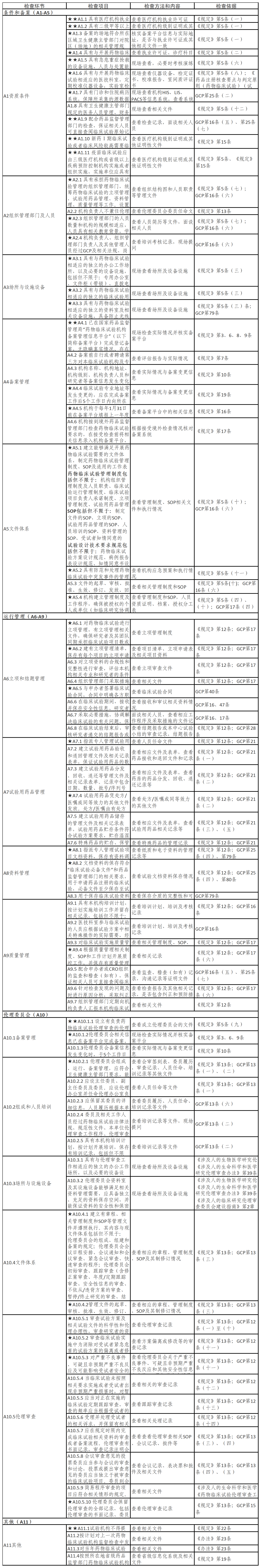
注:1.机构现场检查内容包括11个检查环节、78个检查项目,其中关键项目9项,主要项目31项,一般项目38项。对于新备案且未承担药物临床试验的机构进行监督检查,检查内容包括 44个检查项目(不涉及A6-A9,A10.5),其中关键项目9项,主要项目19项,一般项目16项。
2.本表中所指的研究者为主要研究者。
附表2
京津冀药物临床试验机构监督检查标准——专业部分(B表)

注:1.专业现场检查内容包括8个检查环节和69个检查项目,其中关键项目5项、主要项目28项、一般项目36项。对于新备案且未承担药物临床试验的专业进行监督检查,检查内容包括24个检查项目(不涉及B4-B8),其中关键项目3项,主要项目10项,一般项目11项。
2.本表中所指的研究者为主要研究者。

