京药监发〔2022〕340号
各有关单位:
为做好本市医疗器械注册质量管理体系核查工作,根据《医疗器械监督管理条例》(国务院令第739号)、《医疗器械注册与备案管理办法》(国家市场监督管理总局令第47号)、《体外诊断试剂注册与备案管理办法》(国家市场监督管理总局令第48号)和《国家药监局综合司关于印发境内第三类医疗器械注册质量管理体系核查工作程序的通知》(药监综械注〔2022〕13号)、《北京市药品监督管理局关于印发〈北京市医疗器械注册质量管理体系核查工作程序〉的通知》(京药监发〔2022〕148号)等相关规定,结合我市实际,北京市药品监督管理局组织制定了《北京市医疗器械注册质量管理体系优化核查指导原则(试行)》《北京市医疗器械注册质量管理体系核查中止检查指导原则(试行)》,现予印发,自发布之日起施行。
特此通知。
北京市药品监督管理局
2022年12月28日
北京市医疗器械注册质量管理体系优化核查指导原则(试行)
一、目的和依据
为优化医疗器械注册质量管理体系核查工作,减轻企业负担,提高医疗器械审评审批效率,根据《医疗器械监督管理条例》(国务院令第739号)、《医疗器械注册与备案管理办法》(国家市场监督管理总局令第47号)、《体外诊断试剂注册与备案管理办法》(国家市场监督管理总局令第48号)和《国家药监局综合司关于印发境内第三类医疗器械注册质量管理体系核查工作程序的通知》(药监综械注〔2022〕13号)、《北京市药品监督管理局关于印发〈北京市医疗器械注册质量管理体系核查工作程序〉的通知》(京药监发〔2022〕148号)、《北京市食品药品监督管理局关于印发〈北京市医疗器械快速审评审批办法〉的通知》(京食药监械监〔2018〕4号)等规定,结合实际,制定本指导原则。
二、适用范围
本指导原则适用于北京市药品监督管理局组织的第二、三类医疗器械注册质量管理体系核查(以下简称注册核查)工作,不适用医疗器械注册申请人委托其他企业生产医疗器械,以及医疗器械注册申请人开展注册自检的注册核查。
三、判定原则
(一)对于第二类医疗器械产品注册核查事项,符合以下情形之一,且产品生产地址、生产条件无变化的,原则上可不启动核查:
1.注册申请人未在医疗器械注册证有效期届满6个月前申请延续注册,按照首次注册办理,且产品无变化的;
2.注册申请人申报的医疗器械变更注册事项的变化内容不涉及生产工艺变化的;
3.产品曾申报注册,并在此次申报2年内通过原申报产品的注册核查,因注册申请人原因撤回注册申请,且产品无变化的。
(二)符合以下情形之一,产品生产地址无变化的,启动注册核查,原则上可免于现场检查:
1.对于第三类医疗器械产品注册核查事项,产品曾申报注册,并在此次申报2年内通过原申报产品的注册核查,因注册申请人原因撤回注册申请,且产品生产条件、生产工艺无变化的;
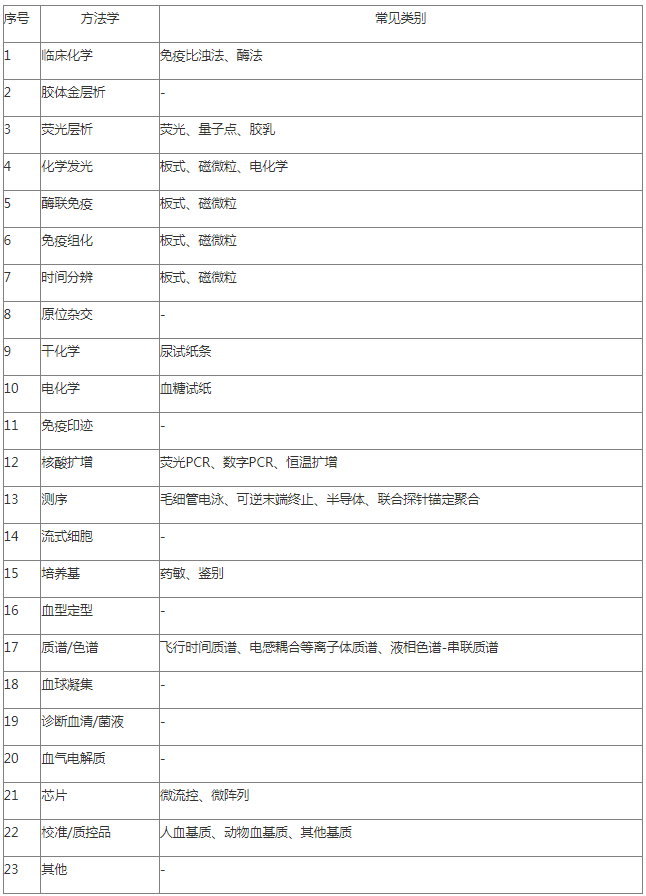
2.已取得生产许可证的第二类医疗器械注册申请人,申请注册的体外诊断试剂与注册申请人已取得医疗器械注册证书产品属于附表1中同一方法学的,或申请注册的医疗器械与注册申请人已取得医疗器械注册证书产品属于《医疗器械分类目录》中同一二级子目录的;
3.对于2年内已通过至少1次医疗器械注册质量管理体系现场核查的注册申请人,且此次申报注册核查的第二类/第三类医疗器械产品与注册申请人已通过检查产品的生产条件和工艺进行对比,具有相同的工作原理、预期用途,并且具有基本相同的结构组成、生产条件、生产工艺的。
(三)对第二类/第三类医疗器械注册申请人2年内通过至少1次医疗器械注册质量管理体系现场核查的注册申请人,产品生产地址无变化的,原则上可优化现场检查项目,重点对用于注册的检验用产品和临床试验产品开展真实性核查(以下简称真实性核查,内容见附表2)。
(四)符合以下情形之一的,原则上不得免于或优化现场检查:
1.注册申请人在2年内存在违反国家有关医疗器械法规规章,被依法立案查处的;
2.北京市企业信用平台即时显示失信企业的;
3.注册申请人处于停产状态的。
四、工作要求
(一)不启动核查
北京市医疗器械审评检查中心(以下简称器械审查中心)在技术审评过程中按照风险管控的原则,认为可不启动核查的,明确不启动核查的理由,不启动核查。
(二)免于现场检查
对于可免于现场检查的,器械审查中心应当按照风险管控的原则,启动核查,明确免于现场检查的理由,认为不能免于现场检查的,应当组织开展现场检查。
对于免于现场检查的,器械审查中心应当将免于现场检查的企业名称及产品名称、免于检查的具体理由告知属地管辖分局。
(三)优化现场检查
对于可优化现场检查的,器械审查中心应当按照风险管控的原则,启动核查,明确优化现场检查的具体理由,重点开展真实性核查;认为不能优化现场检查的,组织开展现场检查。
真实性核查的检查内容应当按照附表1的内容逐项开展检查,重点查阅设计开发过程实施策划和控制的相关记录,用于产品生产的采购记录、生产记录、检验记录和留样观察记录(如适用)等。
现场检查过程中仍应开展对厂区的现场巡视,对检查过程中发现的不符合项目,应当如实记录。
检查组在开展真实性核查时,结合相关检查标准的对应条款进行判定。

北京市医疗器械注册质量管理体系核查中止检查指导原则(试行)
一、目的和依据
为进一步规范医疗器械注册质量管理体系核查工作,保障注册核查工作的严肃性和有效性,根据《医疗器械监督管理条例》(国务院令第739号)、《医疗器械注册与备案管理办法》(国家市场监督管理总局令第47号)、《体外诊断试剂注册与备案管理办法》(国家市场监督管理总局令第48号)和《国家药监局综合司关于印发境内第三类医疗器械注册质量管理体系核查工作程序的通知》(药监综械注〔2022〕13号)、《北京市药品监督管理局关于印发〈北京市医疗器械注册质量管理体系核查工作程序〉的通知》(京药监发〔2022〕148号)等规定,结合实际,制定本指导原则。
二、适用范围
本指导原则适用于北京市药品监督管理局(以下简称市药监局)组织的第二、三类医疗器械注册质量管理体系核查工作。
三、判定原则
开展现场检查过程中出现以下情形,应当中止检查:
(一)因不可抗力等客观因素限制难以继续开展检查的;
(二)发现注册申请人涉嫌存在隐瞒真实情况或者提供虚假信息等违法行为的;
(三)符合中止检查的其他情形。
四、工作要求
(一)中止检查的决定
对符合中止检查原则的,检查组组长应当组织检查组内部沟通,形成检查组意见,向注册申请人通报检查情况,注册申请人进行确认。
拟中止检查的,检查组组长应当充分取证,及时向北京市医疗器械审评检查中心(以下简称器械审查中心)报告。经器械审查中心批准同意后,方可中止检查。
(二)中止检查的记录
中止检查的,检查组应当在检查记录中如实、详细地记录中止检查的原因。
(三)中止检查的处理
中止检查的,检查组应当将检查资料及时交回器械审查中心,暂缓安排检查。待满足继续开展检查条件时,由注册申请人向器械审查中心提出恢复检查申请,由器械审查中心另行安排检查。延迟核查的时间不计入工作时限。
跨省委托生产涉及中止检查的,市药监局应当与相应省级药品监督管理部门互通情况。
第二类医疗器械注册核查涉及中止检查的,器械审查中心应当向市药监局报告;第三类医疗器械注册核查涉及中止检查的,器械审查中心应当向国家药品监督管理局医疗器械技术审评中心报告。
涉及注册申请资料虚假或其他与申报产品相关违法情形的,由器械审查中心作出“未通过核查”的结论,提出不予注册的审评意见,市药监局作出不予注册的许可决定,并按照相关规定进行移交。


