公告〔2021〕51号
为深入贯彻落实《北京市优化营商环境条例》,持续优化营商环境,按照我市推行告知承诺审批制改革工作的要求,自2021年12月27日起,对医疗器械产品出口销售证明、第一类体外诊断试剂备案新办、第一类体外诊断试剂变更备案、第一类体外诊断试剂注销备案、第一类体外诊断试剂备案凭证遗失补办、第二类医疗器械经营备案凭证办理、第二类医疗器械经营备案凭证变更、第二类医疗器械经营备案凭证补发等8个事项(具体情况见附表)实行告知承诺制改革,现将有关事项通知如下:
一、申请办理上述事项的,由申请人向审批部门提交加盖公章的《告知承诺书》和申请材料,承诺符合办理条件并承担违反承诺的相应后果。审批部门经审查申请材料齐全、符合法定形式的,当场作出行政许可或备案决定。
对2021年12月26日(含)前提出上述事项申请的,按照原程序办理。
二、申请人应认真履行承诺内容,按照规定的条件、标准和技术要求从事生产经营活动。对于发现申请人作出虚假承诺,通过提供伪造变造的证件证明(含相关人员)、虚假数据和资料或者采取其他手段骗取行政许可或备案的,将依据《北京市优化营商环境条例》《北京市政务服务事项告知承诺审批管理办法》的规定进行处理。
特此通告。
附件:实施告知承诺制改革事项清单
北京市药品监督管理局
2021年12月23日
附件
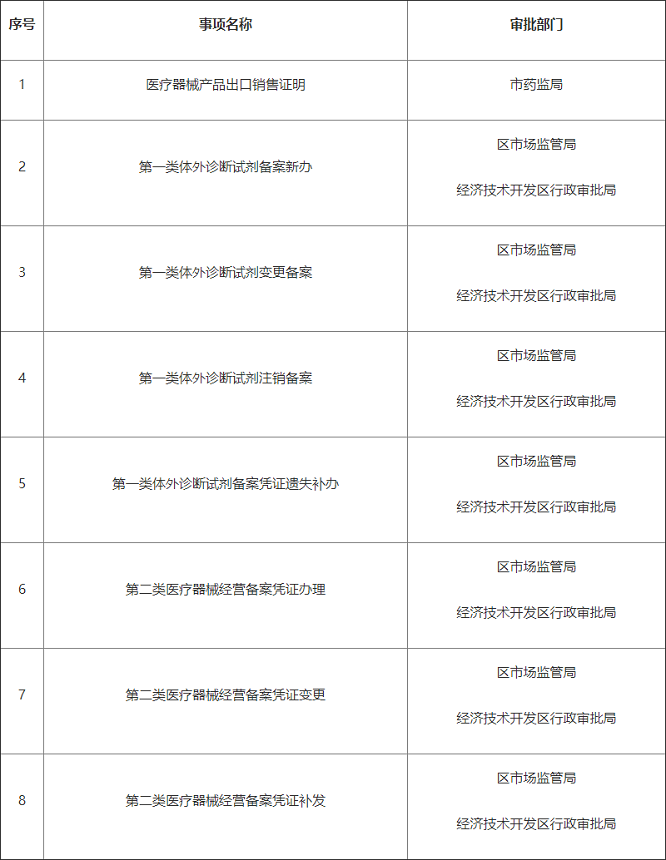
实施告知承诺制改革事项清单