京藥監發〔2026〕78號
各有關單位:
為進一步規範醫療器械出口銷售證明的出具與管理,優化醫療器械出口服務流程,助力北京市醫療器械産業國際化發展,北京市藥品監督管理局結合工作實際及相關政策法規變化,制定了《北京市醫療器械出口銷售證明管理規定實施細則》,經2026年第5次局長辦公會議討論通過,現予以印發,自2026年5月1日起施行。
北京市藥品監督管理局
2026年4月29日
北京市醫療器械出口銷售證明管理規定實施細則
第一章 總則
第一條 為支援醫療器械出口貿易,規範醫療器械出口銷售證明的出具與管理,依據《醫療器械出口銷售證明管理規定》(國家藥品監督管理局2025年第126號公告),結合北京市醫療器械監管實際,制定本細則。
第二條 本細則適用於北京市醫療器械註冊人、備案人、已取得醫療器械生産許可證或者已辦理醫療器械生産備案的生産企業(以下統稱申請人)申請出具醫療器械出口銷售證明,以及北京市藥品監督管理局(以下簡稱市藥監局)開展醫療器械出口銷售證明的服務性事項辦理。
第三條 市藥監局加強醫療器械出口銷售證明資訊化建設,提高智慧化監管服務工作水準。
第四條 申請人應當嚴格落實企業主體責任,加強醫療器械出口品質管理,保證所出口的産品符合進口國家(地區)的要求,並承擔相應法律責任。
第二章 職責劃分
第五條 市藥監局負責制定本市醫療器械出口銷售證明辦理程式,辦理醫療器械出口銷售證明,開展相關資訊公開、公示失效、作廢等工作。
第六條 各區市場監督管理局、市藥監局各分局(以下統稱轄區藥品監管部門)負責對轄區申請人的現場檢查,以及市藥監局交辦的其他相關工作。
第三章 醫療器械出口銷售證明辦理
第七條 擬出口已在中國境內註冊或者備案的醫療器械的,由北京市醫療器械註冊人、備案人作為申請人,向市藥監局提交下列資料,申請出具《醫療器械出口銷售證明(I)》,證明該産品已准許在中國境內生産和銷售:
(一)醫療器械出口銷售證明申請表;
(二)醫療器械註冊證複印件或者産品備案憑證/備案編號告知書複印件;
(三)醫療器械生産許可證正、副本複印件或者生産備案憑證/備案編號告知書複印件(生産地址須與資料(二)中的生産地址一致)。
第八條 擬出口未在中國境內註冊或者備案的醫療器械的,由擬出口産品的北京市實際生産企業作為申請人,向市藥監局提交下列資料,申請出具《醫療器械出口銷售證明(II)》,證明該産品在中國境內按照醫療器械管理但未在中國境內註冊或者備案,該生産企業具有符合醫療器械生産品質管理規範要求的生産條件:
(一)醫療器械出口銷售證明申請表;
(二)醫療器械生産許可證正、副本複印件或者生産備案憑證/備案編號告知書複印件;
(三)醫療器械生産許可證或者生産備案憑證載明的生産範圍包含本類産品所在子目錄和一級産品類別的説明;對於體外診斷試劑,還應當説明擬出口的産品與所生産的産品具有相同的方法學;
(四)生産企業符合生産品質管理規範要求的情況説明或者佐證材料,包括但不限于企業最近一次生産品質管理體系自查報告、企業取得第三方認證機構出具的醫療器械生産品質管理體系認證證書等。
第九條 申請人應當誠實守信,保證提交的資料真實、合法、準確、完整和可追溯。
第十條 申請醫療器械出口銷售證明的資料可以通過聯網核查的,無需申請人提供。
第十一條 對於申請出口已在中國境內註冊或者備案的醫療器械的,市藥監局負責對申請人申報資料的真實性、合法性、有效性進行審核。申報材料符合要求的,市藥監局予以出具醫療器械出口銷售證明;不符合要求的,不予出具。
對於申請出口未在中國境內註冊或者備案的醫療器械的,市藥監局負責對申請人申報資料的真實性、合法性、有效性進行初審;初審符合要求的,將申請材料轉交申請人所屬轄區藥品監管部門。市藥監局結合轄區藥品監管部門對生産企業是否符合生産品質管理規範的檢查意見,綜合評價認為符合生産品質管理規範等要求的,市藥監局予以出具出口銷售證明;不符合生産品質管理規範等要求的,不予出具。
第十二條 轄區藥品監管部門接到市藥監局移轉的申請材料後,應當對申請人的申報材料進行檢查;有屬於本細則第十一條規定情形的應當開展現場檢查;符合要求的作出申請人符合生産品質管理規範的檢查意見;不符合要求的,作出申請人不符合生産品質管理規範的檢查意見。
第十三條 申請人具有下列情形之一的,轄區藥品監管部門應當組織現場檢查:
(一)申請資料存疑需要現場核實;
(二)申請出口的産品(含與申請出口的同類産品)抽檢不合格未完成整改,或不良事件監測中發現嚴重不良事件未完成評價和整改;
(三)醫療器械生産分級監管中生産企業品質管理體系風險為四級且近一年未接受過品質管理體系全項目檢查;
(四)處於停産狀態或未完成停産整改;
(五)其他有必要開展現場檢查的。
第十四條 轄區藥品監管部門按照醫療器械生産品質管理規範相關檢查指導原則進行檢查,綜合評價並提出檢查意見。檢查結果判定為“未通過檢查”的,或在規定期限內未完成整改的,出具生産品質管理規範不符合要求的意見。審查發現申請資料真實性存在問題,應當將有關情況報告市藥監局。
對於同時申請第一類醫療器械和第二、三類醫療器械出口銷售證明的申請人,需要現場檢查時,由市藥監局相關分局會同相關區藥品監管部門聯合開展檢查和整改復查。
第十五條 申請人具有下列情形之一的,不予出具醫療器械出口銷售證明並説明理由:
(一)被列入市場監督管理嚴重違法失信名單;
(二)提供虛假申請資料或者申請資料不符合要求的;
(三)因違反醫療器械監督管理相關規定,處於責令停産整改狀態、涉案處理期間的;
(四)認定為不符合生産品質管理規範等要求的。
第十六條 申請已在中國境內註冊或者備案醫療器械出口銷售證明的辦理時限為自受理之日起1個工作日。申請未在中國境內註冊或者備案醫療器械出口銷售證明的辦理時限為自受理之日起5個工作日。開展現場檢查以及企業整改時間不計入時限。
第十七條 醫療器械出口銷售證明的中文編號方式為:京藥監械出X1X2號,英文編號方式為:No.MDBJX1X2。其中:X1為出具證明的年份(4位);X2為流水號(6位)。
第十八條 醫療器械出口銷售證明有效日期不應超過申請人申報資料中各類證件最先到達的截止日期。第一類醫療器械的出口銷售證明有效期不超過3年。
第十九條 醫療器械出口銷售證明的電子證明與紙質證明具有同等效力。
第四章 醫療器械出口銷售證明管理
第二十條 應當落實品質管理體系要求,建立並保存相關品質管理文件和記錄、已辦理的出口銷售證明、包裝、産品説明書和標簽樣式、報關單、數量、産值、進口國家(地區)等相關資料,保證醫療器械出口過程可追溯。
第二十一條 醫療器械出口銷售證明有效期屆滿或者載明內容發生變化的,申請人應當重新申請。
第二十二條 醫療器械註冊證或者産品備案、醫療器械生産許可證或者生産備案被依法吊銷、撤銷、登出或者取消的,相應的出口銷售證明應當自吊銷、撤銷、登出或者取消之日起失效,市藥監局在公開的醫療器械出口銷售證明相關資訊中標注失效。
第二十三條 醫療器械出口銷售證明有效期屆滿前,申請人發現不再符合相關出具證明條件的,應當向所屬轄區藥品監管部門報告。轄區藥品監管部門應當及時將相關情況報告市藥監局,市藥監局對已出具的相關出口銷售證明予以公示作廢。
第二十四條 轄區藥品監管部門在監督管理過程中發現申請人存在第十四條所列情況,或者認定其不再符合出具證明條件,或者發現提交的相關資料發生變化且影響到出口銷售證明載明內容需要重新申請的,應當及時將相關情況報告市藥監局,市藥監局對已出具的相關出口銷售證明予以公示作廢。
第二十五條 申請人通過提供虛假資料或者採取其他欺騙手段騙取出口銷售證明,或者變造、偽造出口銷售證明的,市藥監局對已出具的出口銷售證明予以公示作廢,並在信用檔案中記錄,5年內不再為其出具出口銷售證明。涉嫌違法犯罪的,依法移交相關部門處理。
第二十六條 市藥監局將醫療器械出口銷售證明資訊在資訊産生後7個工作日內進行公開,並在資訊産生後15個工作日內將其按照相關要求報送國家藥品監督管理局資訊中心。
第五章 附則
第二十七條 本細則由市藥監局負責解釋。
第二十八條 本細則自2026年5月1日起施行。
附件1
醫療器械出口銷售證明申請表
(格式)
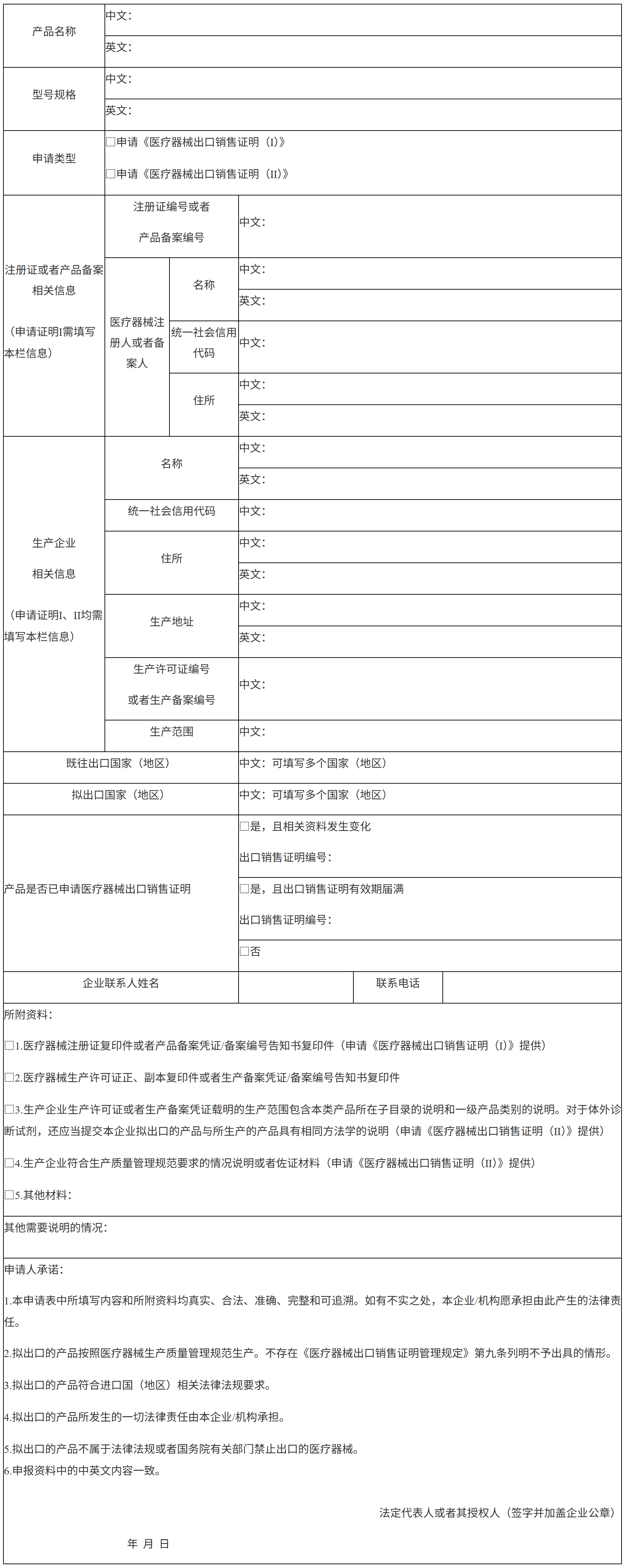
注:
1.申請表填寫內容應當真實、完整、準確,不得塗改。
2.擬出口已在中國境內註冊或者備案的醫療器械和未在中國境內註冊或者備案的醫療器械,應當分別提交申請表。
3.按照《醫療器械出口銷售證明管理規定》報送資料,報送的資料應當按照規定中的順序排列並標明序號。
4.申請表中填寫的産品資訊和企業資訊應當與醫療器械註冊證、生産許可證載明內容,或者備案資訊一致。
5.對於單次申請辦理多個産品、單個産品的型號規格較多等情形,申請表相應欄目可以註明“見附頁”,附頁上應當加蓋企業公章。
6.如有其他情況,如因命名規則等原因導致的産品中英文名稱差異,或者需要列明品牌名稱、商品名、貨號、産品編碼、産品目錄號、廠商識別代碼等,請在申請表的“其他需要説明的情況”欄中寫明具體內容。
附件2
中華人民共和國
PEOPLE’S REPUBLIC OF CHINA
醫療器械出口銷售證明(I)
CERTIFICATE FOR EXPORTATION OF MEDICAL DEVICE(I)
(格式)
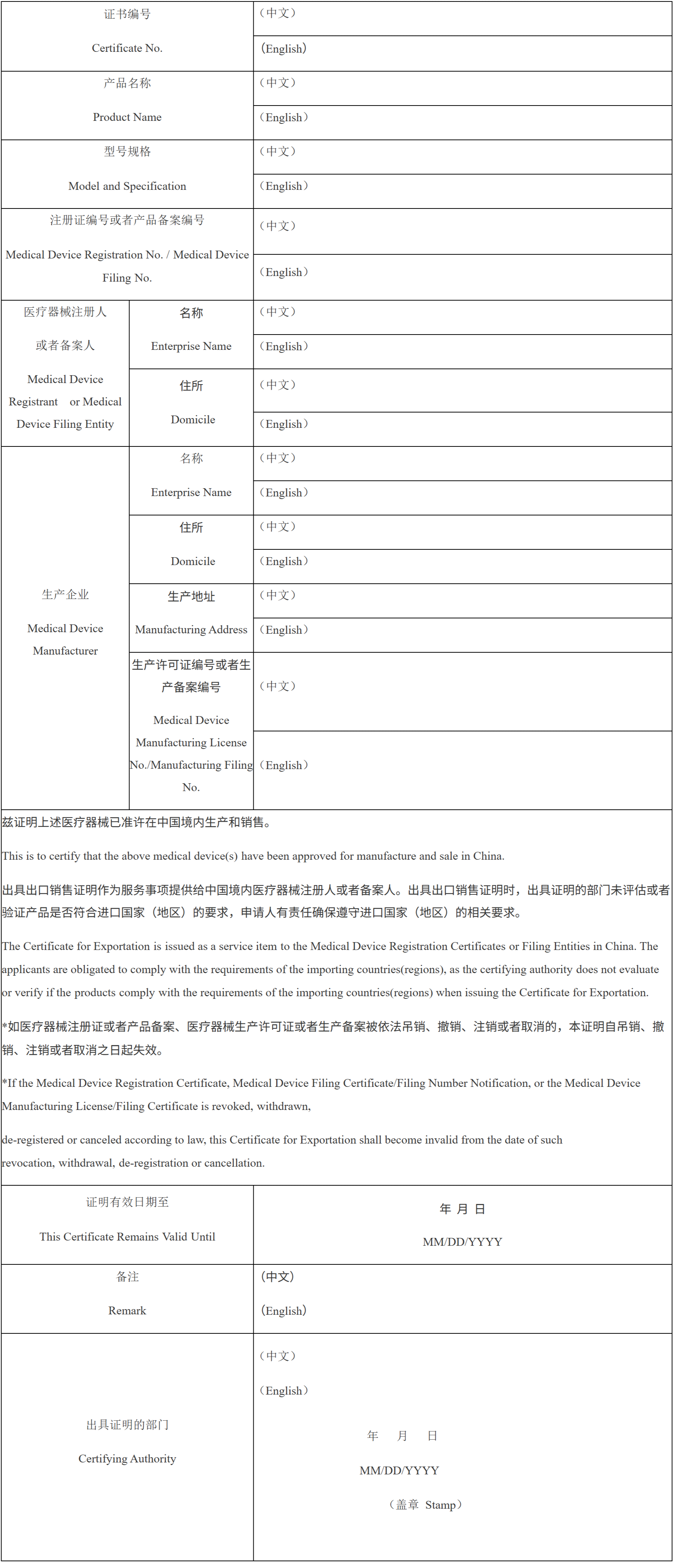
附件3
中華人民共和國
PEOPLE’ S REPUBLIC OF CHINA
醫療器械出口銷售證明(II)
CERTIFICATE FOR EXPORTATION OF MEDICAL DEVICE(II)
(格式)


