公告〔2021〕51號
為深入貫徹落實《北京市優化營商環境條例》,持續優化營商環境,按照我市推行告知承諾審批制改革工作的要求,自2021年12月27日起,對醫療器械産品出口銷售證明、第一類體外診斷試劑備案新辦、第一類體外診斷試劑變更備案、第一類體外診斷試劑登出備案、第一類體外診斷試劑備案憑證遺失補辦、第二類醫療器械經營備案憑證辦理、第二類醫療器械經營備案憑證變更、第二類醫療器械經營備案憑證補發等8個事項(具體情況見附表)實行告知承諾制改革,現將有關事項通知如下:
一、申請辦理上述事項的,由申請人向審批部門提交加蓋公章的《告知承諾書》和申請材料,承諾符合辦理條件並承擔違反承諾的相應後果。審批部門經審查申請材料齊全、符合法定形式的,當場作出行政許可或備案決定。
對2021年12月26日(含)前提出上述事項申請的,按照原程式辦理。
二、申請人應認真履行承諾內容,按照規定的條件、標準和技術要求從事生産經營活動。對於發現申請人作出虛假承諾,通過提供偽造變造的證件證明(含相關人員)、虛假數據和資料或者採取其他手段騙取行政許可或備案的,將依據《北京市優化營商環境條例》《北京市政務服務事項告知承諾審批管理辦法》的規定進行處理。
特此通告。
附件:實施告知承諾制改革事項清單
北京市藥品監督管理局
2021年12月23日
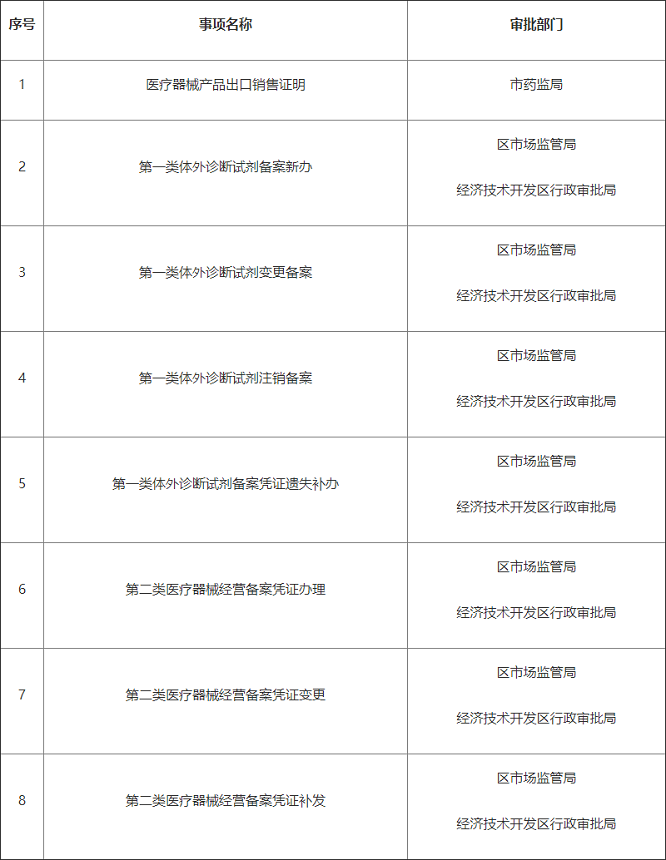
附件
實施告知承諾制改革事項清單